legge di boyle
Nel 1662 Robet Boyle formulò una legge sui gas nota come legge di Boyle olegge dell'isoterma: il volume occupato da un gas, mantenuto a temperatura costante, è inversamente proporzionale alla pressione alla quale il gas è sottoposto.
Ciò vuole dire che, mantenendo costante la temperatura e raddoppiando, triplicando o quadruplicando la pressione esercitata sul gas, il suo volumediventa rispettivamente un mezzo, un terzo, un quarto.
In termini matematici, la legge di Boyle può essere espressa nel seguente modo:
P1 · V1 = P2 · V2
in cui:
P1 e V1 sono rispettivamente la pressione e il volume iniziali
P2 e V2 sono rispettivamente la pressione e il volume finali
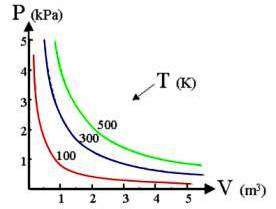
In un sistema di assi cartesiani la curva che si ottiene ponendo i valori (calcolati alla medesima temperatura) del volume in ascissa e della pressione in ordinata, è una iperbole equilatera detta isoterma. Diminuendo la temperatura, l'isoterma si sposta verso l'interno:
Ciò vuole dire che, mantenendo costante la temperatura e raddoppiando, triplicando o quadruplicando la pressione esercitata sul gas, il suo volumediventa rispettivamente un mezzo, un terzo, un quarto.
In termini matematici, la legge di Boyle può essere espressa nel seguente modo:
P1 · V1 = P2 · V2
in cui:
P1 e V1 sono rispettivamente la pressione e il volume iniziali
P2 e V2 sono rispettivamente la pressione e il volume finali
In un sistema di assi cartesiani la curva che si ottiene ponendo i valori (calcolati alla medesima temperatura) del volume in ascissa e della pressione in ordinata, è una iperbole equilatera detta isoterma. Diminuendo la temperatura, l'isoterma si sposta verso l'interno: